
20世紀下半葉TIL療法問世,并在多個癌種中取得療效突破,2024年全球首款TIL療法獲得美國FDA批準上市。同其他免疫細胞療法相比,TIL療法在實體瘤治療中具有高特異性、高安全性、廣譜抗癌、療效持久等優勢,并可與其他療法協同聯用,獲取更大治療收益。TIL療法已成為當前實體瘤免疫治療領域極具競爭力和產業化潛力的治療新技術。
2024年12月18日,弗若斯特沙利文(Frost & Sullivan,以下簡稱“沙利文”)于“智造領航”2024-TIL產業化峰會上正式發布《腫瘤浸潤淋巴細胞(TIL)療法行業現狀與發展趨勢白皮書》(以下簡稱《白皮書》),報告旨在對TIL療法行業進行全面深入分析,從政策法規、產業發展、市場需求、產品管線、技術創新等多方面探究行業發展背后的驅動因素,挖掘行業發展巨大潛力,追蹤行業未來發展趨勢。
掃描二維碼立即獲取報告

《腫瘤浸潤淋巴細胞(TIL)療法行業現狀與發展趨勢白皮書》從惡性腫瘤的流行病學特征及治療方式入手,介紹了腫瘤免疫療法的發展及分類,并將TIL療法與其他抗腫瘤治療代表類型的藥物及其他過繼性T細胞療法進行了對比分析,系統闡述了TIL療法的發展歷程和在實體瘤領域的治療優勢,展現了TIL療法現階段的主要挑戰以及領先企業的應對方式,分析了已上市TIL療法產品以及當前在研管線,并深入剖析了TIL療法市場的未來發展趨勢。
下文為白皮書部分節選,詳細內容可掃描二維碼獲取完整版:
抗腫瘤治療市場概覽
01 全球及中國腫瘤發病人數分析
全球及中國癌癥死亡及新發病例中,實體腫瘤占據大多數。據國際癌癥研究機構(International Agency for Research on Cancer,IACR)數據顯示,2022年發病率最高的五種癌癥均為實體瘤,占全球癌癥總體發病的45%以上,此外實體瘤也是導致癌癥相關死亡的主要原因。實體瘤通常生長速度較快,并伴隨侵襲局部組織及遠處轉移的特點。實體瘤患者多在晚期才得以確診,預后不佳,已成為全球范圍內的主要疾病負擔之一,目前仍缺乏有效的治療手段。
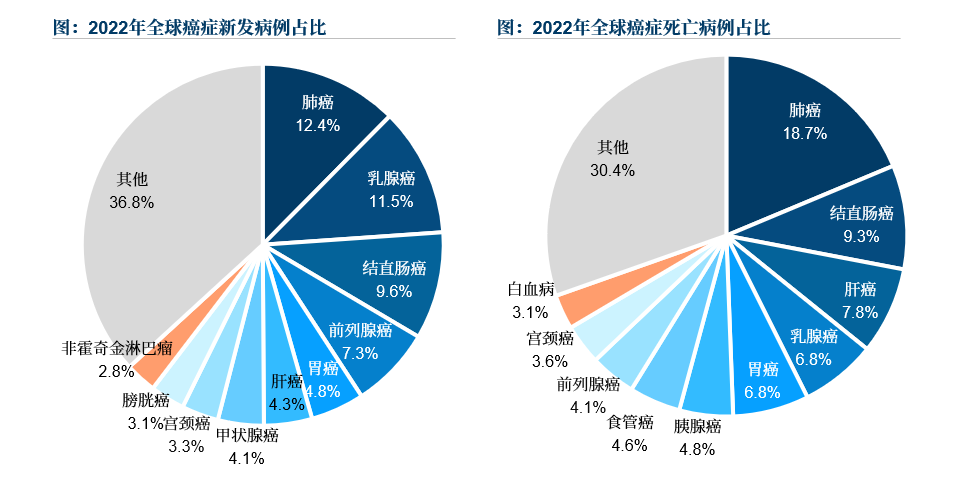
來源:文獻檢索,沙利文分析
02 代表性抗腫瘤治療方式分析
隨著人類對于腫瘤認知的不斷深入,從腫瘤組織到細胞再到基因層面,腫瘤治療方式也在不斷革新,從手術、放化療、靶向藥再到最新的免疫療法,人們開發出越來越多的腫瘤治療方式,同時腫瘤患者預后也在不斷改善。
03 全球及中國抗腫瘤藥物市場分析
近年來癌癥發病率不斷提升,全球范圍內對于抗腫瘤藥物的臨床需求日益增加,隨著癌癥診療技術的提升,抗腫瘤藥物市場規模正在逐漸擴大。根據弗若斯特沙利文數據分析,全球抗腫瘤藥物市場規模已經從2019年的1,435億美元增長到2023年的2,289億美元,預計到2030年,全球抗腫瘤藥物市場規模將達到4,198億美元。中國抗腫瘤藥物市場規模從2019年的1,827億元增長至2023年的2,416億元,期間年復合增長率為7.2%,預計中國抗腫瘤藥物市場在2030年將會達到人民幣5,484億元,2023-2030年的年復合增長率為12.4%。同全球抗腫瘤藥物市場增速相比,中國2023-2030年增速更快,并有望繼續保持穩步增長的態勢。
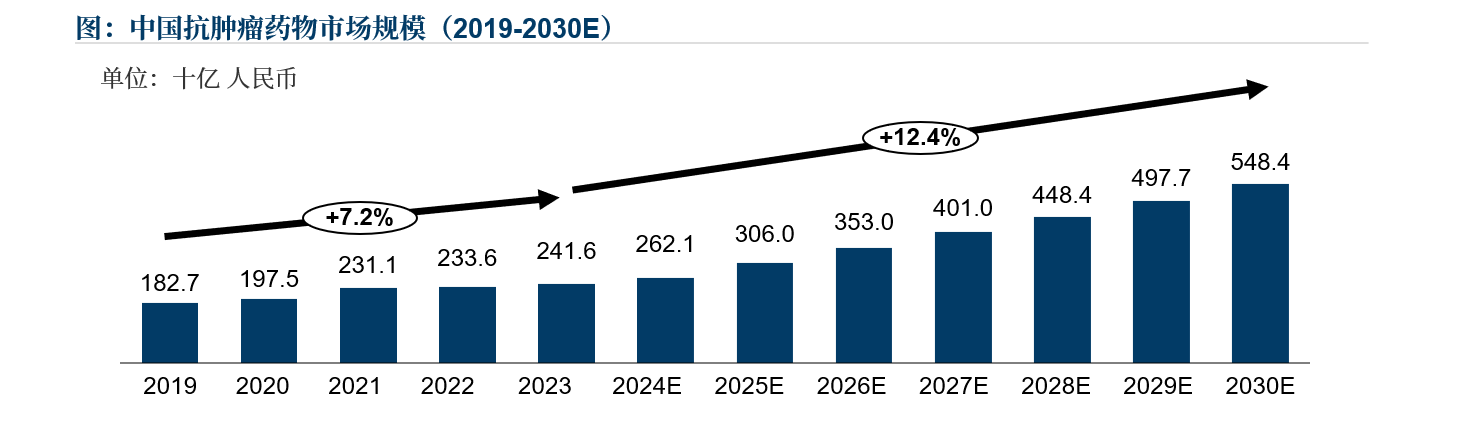
來源:沙利文分析
據弗若斯特沙利文數據分析,2023年中國抗腫瘤藥物市場以化療藥物為主,占整體抗腫瘤藥物市場的47.5%,未來隨著靶向藥物和免疫治療藥物的上市和普及,中國相關藥物的市場占有率有望進一步提升。據弗若斯特沙利文數據分析,預計到2030年,中國抗腫瘤藥物市場中,免疫療法的市場份額將得到大幅度提升,預計到2030年達到43.9%,成為中國抗腫瘤藥物市場的主力軍,支撐中國抗腫瘤藥物市場規模進一步擴大。
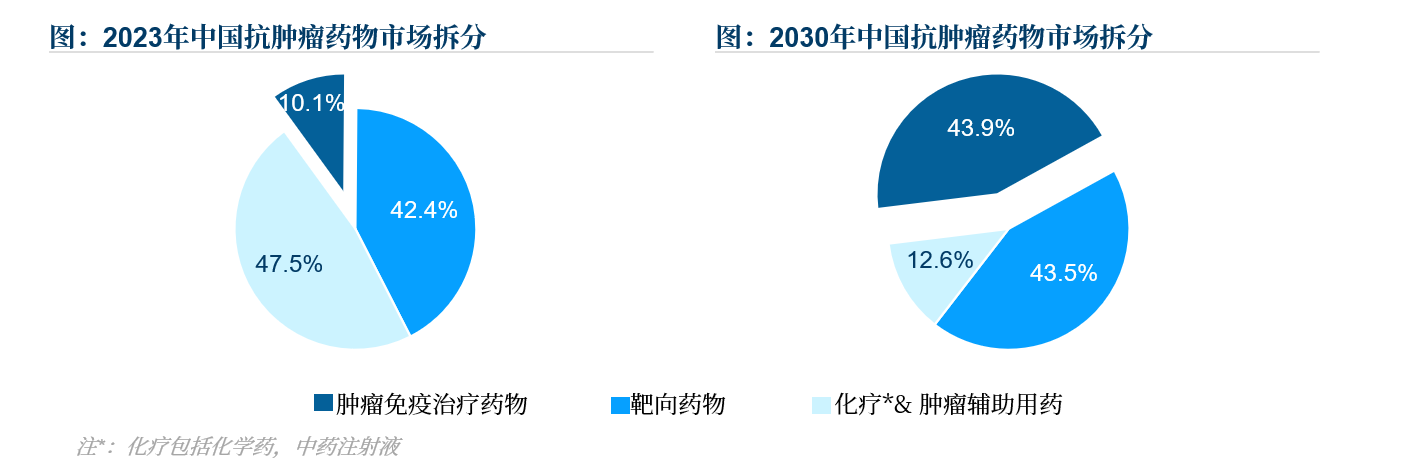
來源:沙利文分析
04 腫瘤免疫療法發展與分類
腫瘤免疫療法(Cancer Immunotherapy)指的是利用人體免疫系統對抗癌癥的方法,發展至今已有超百年歷史,目前已經發展成為繼手術、放化療、靶向藥之后的第四大癌癥治療技術。
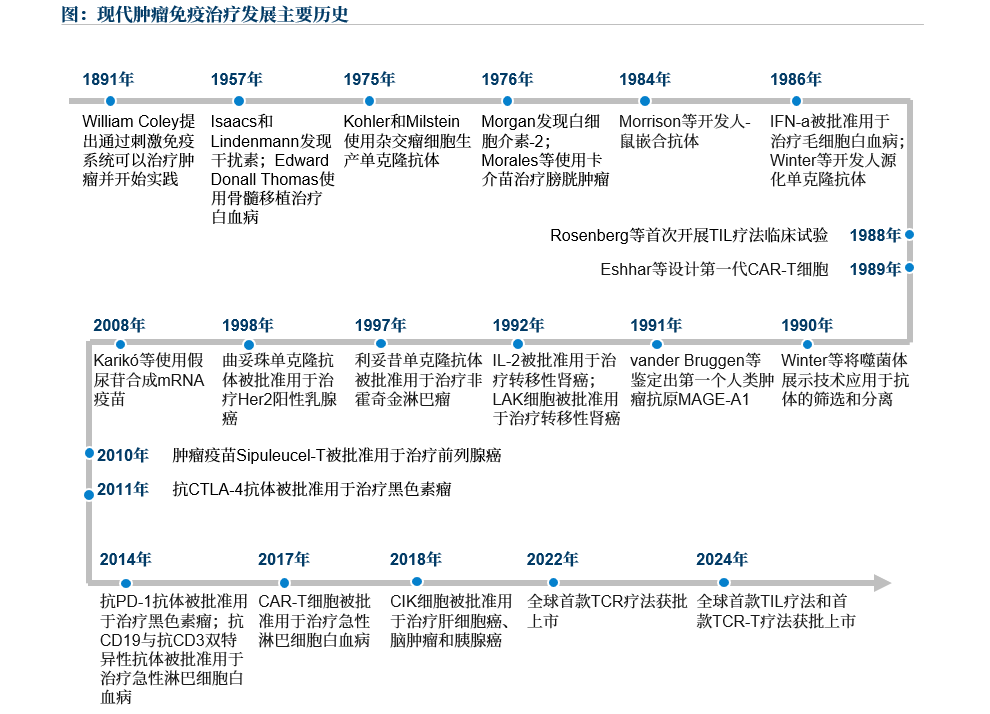
來源:文獻檢索,沙利文分析
T細胞是介導人體細胞免疫的核心細胞類型,目前基于T細胞的過繼性細胞免疫療法主要有腫瘤浸潤淋巴細胞(TIL)療法、T細胞受體基因修飾T細胞(T Cell Receptor T-Cell,TCR-T)療法和嵌合抗原受體T細胞(Chimeric Antigen Receptor T-Cell,CAR-T)療法。CAR-T細胞療法自2017年上市以來,在多種血液腫瘤中均發揮出良好的治療效果;但是目前CAR-T療法在實體腫瘤治療中面臨多重挑戰,仍有待技術的突破。TIL療法所用的細胞主要來源于切除的腫瘤組織,其進入腫瘤微環境能力強,具有天然的多重腫瘤特異性,靶向異質性腫瘤抗原,因此在實體腫瘤中往往可以發揮出更好的治療效果。
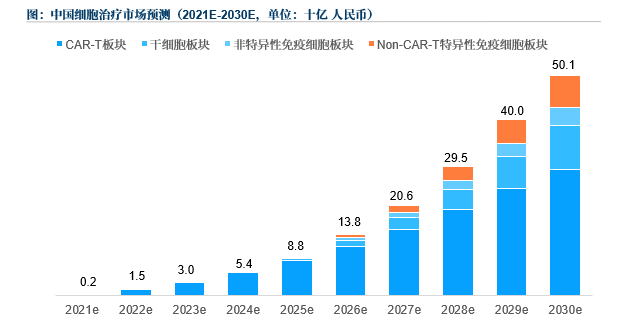
據弗若斯特沙利文數據分析,2025年~2030年,全球細胞治療市場中CAR-T細胞療法的年復合增長率為19.2%,以TIL療法、TCR-T療法為首的其他特異性免疫療法的年復合增長率將達到66.4%。
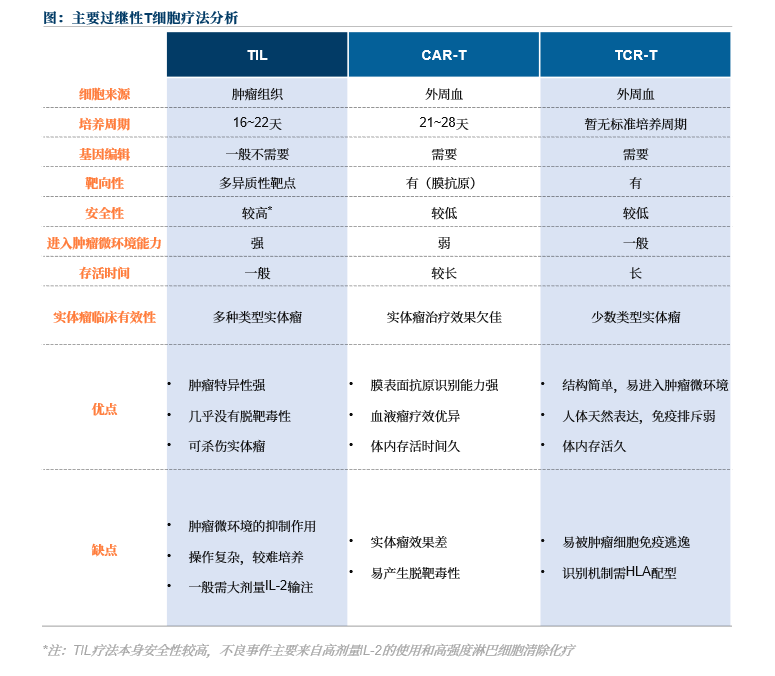
來源:文獻檢索,沙利文分析
TIL療法行業介紹
01 TIL療法發展歷程
20世紀50年代,人們發現了T細胞在移植物抗腫瘤過程中的關鍵作用,這推動人們開始研究T細胞在腫瘤免疫中的作用。1982年,免疫治療先驅史蒂文·羅森伯格(Steven Rosenberg)博士同其美國國立衛生研究院(National Institutes of Health, NIH)同事率先從荷瘤小鼠腫瘤組織中分離出TIL,并在結腸癌模型中發現其可使腫瘤轉移灶縮小,為TIL療法治療晚期惡性腫瘤奠定了基礎。1988年,TIL療法開始了臨床上的首次治療嘗試。隨著技術的成熟和發展,進入21世紀以來,TIL療法獲得廣泛關注并取得了重要的進展,并在2024年迎來首款TIL療法上市。如今TIL療法已經成為抗癌治療中的重要手段,有著極其廣闊的市場前景。
02 TIL療法實體瘤領域治療優勢分析
同其他免疫細胞療法相比,TIL療法在實體瘤治療中具有多重獨特優勢,包括高特異性、高安全性、廣譜抗癌、療效持久等,并可與多療法協同聯用,實現更大治療獲益,TIL療法憑借其在實體瘤治療的優勢獲得多方青睞。

來源:文獻檢索,沙利文分析
03 TIL療法的細胞來源與制備
TIL細胞主要來源于手術腫瘤組織。自TIL療法應用于臨床以來,其制備工藝不斷發展成熟,目前在臨床治療中的安全性和有效性已經得到驗證。早期手術切除的腫瘤組織亦可作為TIL細胞的來源,預先制備TIL種子細胞并凍存,待疾病進展或復發時擴增使用。但這一路徑對TIL細胞活力要求高,需耐受凍存復蘇的不利影響。目前,君賽生物已完成該路徑的驗證,一名高級別腦膠質瘤患者經化療、放療、電場治療、CAR-T療法等失敗,回輸一年前制備的TIL后,僅4周腫瘤已完全消退。
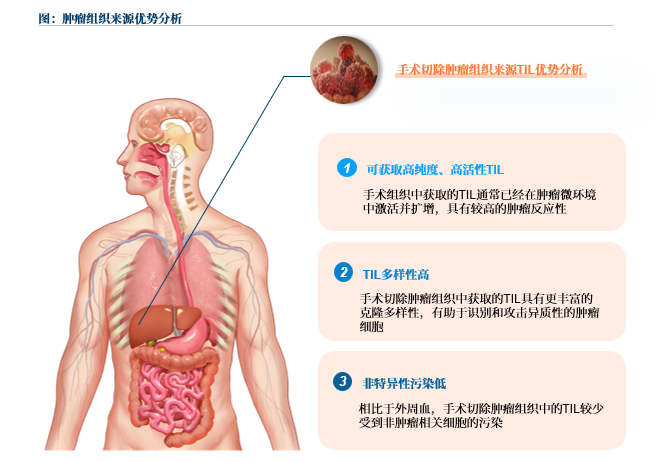
來源:文獻檢索,沙利文分析
目前,通過手術獲取腫瘤組織,再進行TIL分離、擴增等步驟,最后回輸到患者體內進行治療已形成TIL療法常規治療流程,因常規TIL對IL-2有依賴性,TIL回輸前需高強度預處理,回輸后需大劑量IL-2多次輸注。
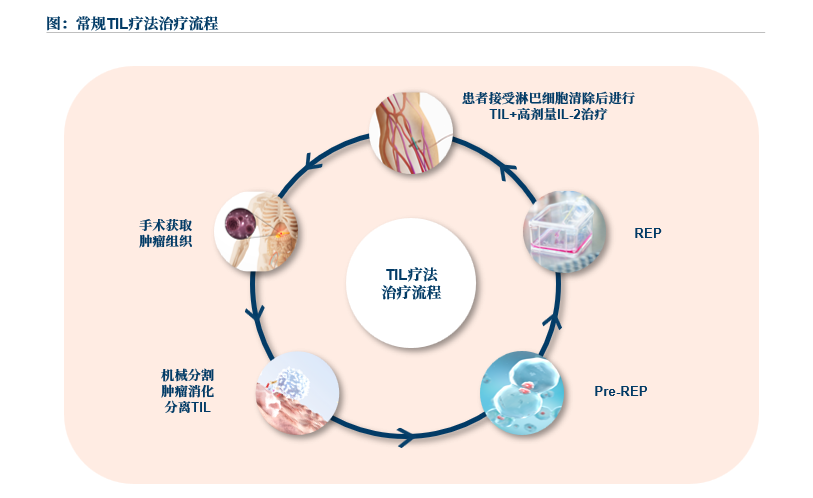
來源:文獻檢索,沙利文分析
04 TIL療法行業挑戰
TIL療法具有天然多克隆和高臨床響應的優勢,其抗腫瘤作用正在各類腫瘤治療中得到積極探索。然而,TIL療法在技術方面仍存在一些挑戰:
如在切除并獲取腫瘤組織后,只有一部分TIL能夠被分離和擴增;常規TIL細胞制備工藝所用的到滋養細胞,來自于健康人的PMBC,經過輻照后使用;滋養細胞的使用帶來了額外成本,增加了引入外源污染的風險,由于一次生產需多人份PBMC,難以進行質量控制,而對獻血的依賴性也造成了供應鏈的風險。
目前,我國細胞治療領域已邁入規范化發展的階段,2024年1月,上海市醫藥質量協會批準并正式發布《細胞治療產品生產用空間密閉系統應用指南》,2024年11月,上海君賽生物科技有限公司聯合中國標準化研究院等多家單位起草的《腫瘤浸潤淋巴細胞(TIL)制劑制備和質量控制指南》已由中國醫藥生物技術協會掛網公示。
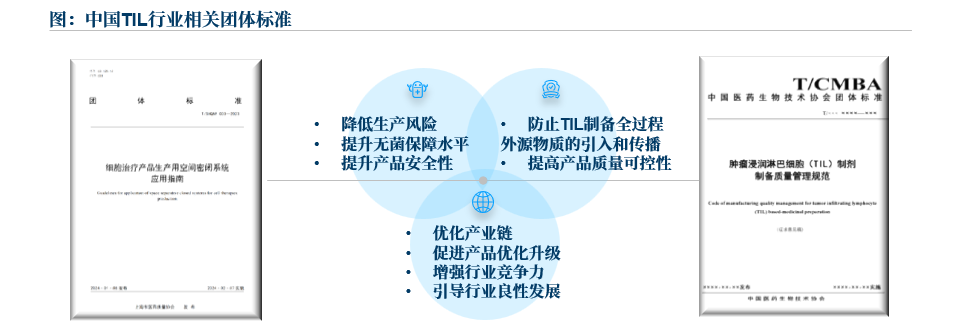
來源:公開資料,沙利文分析
此外,在臨床應用時大劑量環磷酰胺和氟達拉濱預處理及靜脈輸注大劑量IL-2,會引起顯著的毒性。對于晚期腫瘤患者而言存在巨大的負擔,治療時需配備重癥監護,一定程度上限制了TIL療法的臨床應用。2024年5月,君賽生物與上海第十人民醫院婦產科程忠平主任團隊在期刊《BMC Medicine》上發表了創新TIL療法研究成果,該研究開創性地開發了一種低劑量預處理的、未聯用IL-2的天然TIL療法。通過改良TIL療法臨床治療方案,極大地提升了TIL療法的安全性和可及性,對于晚期腫瘤患者,特別是高齡患者或無法耐受高毒性治療的患者提供了有希望的治療選擇。
TIL療法作用機制與傳統靶向藥物開發的思路不同,且成分復雜,因而在審評審批方面存在一定難度。2024年2月,FDA加速批準全球首款TIL療法上市,成為全球首個治療實體瘤的T細胞療法。但其在獲批前,由于尚未明確產品質量檢測項目與客觀臨床療效的相關性,被FDA一再要求提供效力檢測數據,導致BLA遞交延誤。
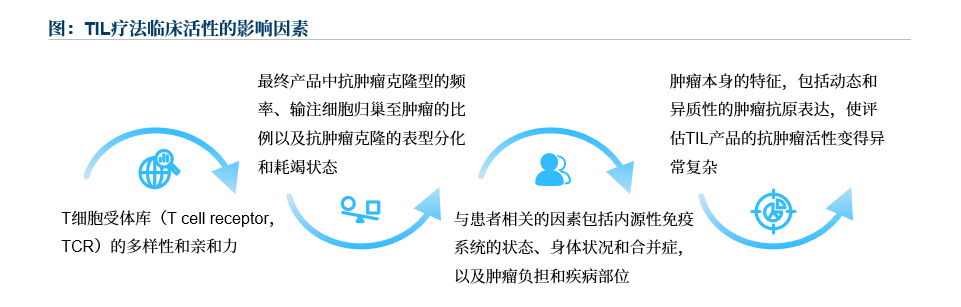
來源:文獻檢索,沙利文分析
TIL療法作為個性化的治療方式,其商業化的推廣和普及需要各部門之間的協調合作,以惠及更多患者。
05 君賽生物新型TIL療法優勢
作為行業內擁有技術創新領先優勢的TIL療法公司,君賽生物的TIL療法具有TIL細胞培養成功率高、數量多、成分組成優異、成本控制好、患者治療門檻低等多重優勢。
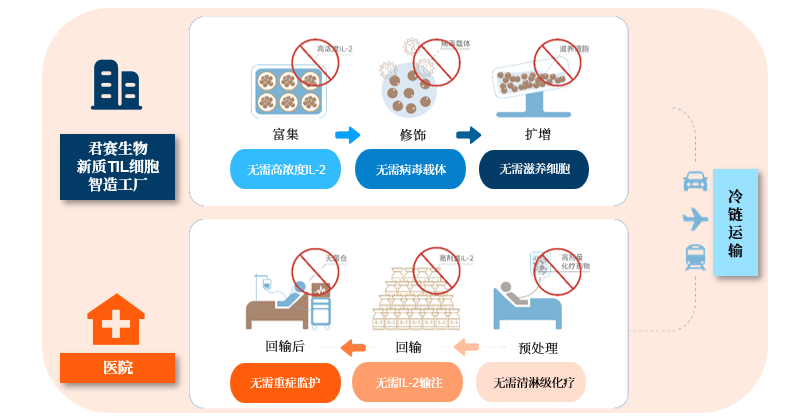
來源:公司資料,沙利文分析
06 TIL療法行業上下游產業鏈分析
近年來伴隨著市場擴大和政策推動,TIL療法行業各環節相互支撐,逐步構建起集采集、存儲、科研、臨床、生產于一體的完整產業鏈。
已上市TIL療法產品及在研管線分析
01 已上市TIL療法分析
2024年2月,美國食品藥品監督管理局(FDA)加速批準Iovance Biotherapeutics公司的TIL療法Lifileucel(商品名:Amtagvi™)上市,用于接受過PD-1抑制劑治療的不可切除或轉移性成年黑色素瘤患者,如果存在BRAF基因V600突變,還需接受過BRAF抑制劑(聯合或不聯合MEK抑制劑)治療。Amtagvi™成為全球首個獲批用于實體腫瘤治療的T細胞療法,實體瘤治療迎來新的精準治療時代。
然而,Lifileucel在臨床應用的過程中存在需要高強度的預處理以及治療相關死亡率高的挑戰,IL-2的高劑量使用對于安全性產生了不良影響。FDA在加速批準Lifileucel上市的同時于商品說明書上添加了黑框警告,提示不良反應。國內外TIL研發公司致力于開發替代策略、降低預處理強度以及避免對IL-2的依賴,推進技術升級,提高臨床治療的安全性。

來源:文獻檢索,沙利文分析
Lifileucel作為全球首款獲批的TIL療法,革命性地改變了實體瘤的治療方式。TIL療法的特性使其在實體瘤治療中有著廣闊的市場前景。
02 TIL療法在研管線分析
近年來全球及中國范圍內TIL療法在研管線數量不斷增加,在實體瘤細胞免疫療法中占比不斷上升。TIL療法正在迅速成為實體瘤細胞免疫療法的熱門研究領域。2020年,TIL療法年度新增管線數量僅占實體瘤領域細胞療法新增管線數量總體的5.6%,而截止到2024年12月,TIL療法占比已經達到20.5%,其也成為實體瘤領域新增管線數量最多的細胞療法。
截至2024年12月,全球共有88條TIL療法管線處于臨床試驗階段,適應癥針對黑色素瘤、非小細胞肺癌、宮頸癌、頭頸部鱗狀細胞癌和卵巢癌等布局較多。
其中用于治療黑色素瘤的產品Lifileucel(LN144)已獲得FDA加速批準,Iovance正繼續積極推進研究,探索將Lifileucel與免疫抑制劑聯用,前移治療線數,并評估其在黑色素瘤以外的其他瘤種中的治療潛力。隨著在研TIL管線的進展與突破,預計未來將會有更多TIL療法進入市場,惠及更多患者。
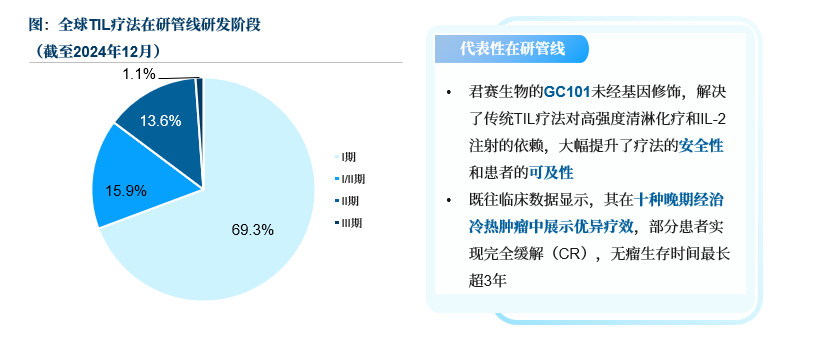
來源:clinicaltrials、CDE(統計截至2024.12),沙利文分析
臨床試驗表明減少對IL-2依賴的治療途徑值得進一步探索。此外由于TIL療法工藝難度大,企業仍需積極調整策略,以應對臨床和研發階段的不確定性。
君賽生物作為中國TIL療法的重點創新企業,通過自主原創的DeepTIL®細胞富集擴增平臺與NovaGMP®非病毒載體基因修飾平臺,公司已開發一系列全球領先的天然TIL及基因修飾TIL細胞新藥,其中2款創新型TIL療法已進入臨床試驗階段,并在10種不同類型晚期實體腫瘤中展現優異臨床療效(包括多線治療失敗的胰腺癌與高級別腦膠質瘤),其中7例患者腫瘤被完全清除,無瘤生存最久時間已超過3年,相關研究結果發表在JITC、BMC Medicine、ASCO、ESMO等國際知名學術期刊或學術會議上。所有患者僅需進行低強度預處理,無需任何劑量IL-2聯用,普通病房即可完成治療,且均未發生治療相關嚴重不良事件。
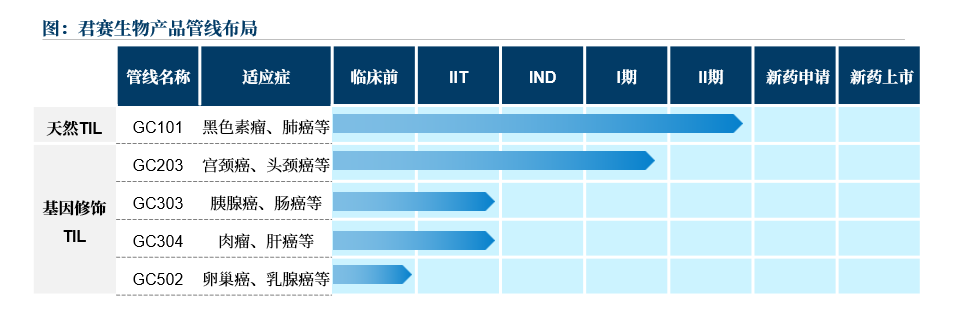
來源:君賽官網,沙利文分析
圍繞提高安全性和有效性兩個方向,TIL療法呈現出多種新的創新研發趨勢。目前TIL療法研發中提高安全性的一個主要方式就是降低IL-2的劑量,或者不使用IL-2。這一方面,君賽通過專有的細胞培養工藝實現完全不使用IL-2,Obsidian通過表達膜結合型IL-15實現完全不使用IL-2,沙礫生物通過表達膜結合型IL-15/IL-15Rα實現使用低劑量IL-2。副作用另一面則源自高強度的清淋化療,針對這一方面,國內君賽已開發低強度預處理方案,同時Obsidian也在探索低強度的預處理方案。
目前改善TIL療法治療的有效性主要從兩個方面展開,一方面為提升TIL本身的治療效果,另一方面則是解決在腫瘤微環境中TIL面對的免疫抑制問題。此外,通過技術的創新突破加速TIL療法產業化和商業化也是研發的重要方向。
TIL療法市場未來發展趨勢分析
01 TIL療法市場驅動因素分析
近年來,TIL療法行業迎來了快速增長,全球及中國TIL療法市場在多維因素共同推動下進入到高速發展階段。2024年首款TIL療法的上市再次助推市場熱情,患者需求、技術創新以及資本投入等逐步轉化為市場發展驅動力,推動行業進一步發展。
中國TIL療法市場的快速增長離不開政策支持以及藥品審批制度改革的推動,政策支持對行業的快速發展起到了關鍵作用,是支持中國TIL療法持續增長的關鍵因素。
02 TIL療法資本市場表現分析
近年來,多家布局TIL療法領域公司上市。全球資本對于TIL療法領域關注度不斷提高,同時更加傾向于創新公司的早期投資,有助于推動TIL療法行業技術創新和臨床推進,加速行業發展。
隨著中國政策的支持、臨床需求的擴大以及中國企業自主創新水平的提高,中國TIL療法領域公司得到來自國內外資本市場的高度關注。相較于2023年,2024中國TIL療法領域公司融資事件進一步增多,并伴隨著投資金額的增加,資本對于行業整體發展預期持樂觀態度。擁有核心技術、在TIL療法領域有創新產品優勢的公司更容易獲得投資。2024年,君賽生物獲得超4億元B輪融資,成為領域內已披露最大金額的投資。隨著TIL療法領域內優秀公司產品的持續推進,臨床試驗數據的進一步披露以及后續產品上市和商業化進程,將有望進一步吸引資本投入,并帶來行業的持續繁榮發展。
03 TIL療法市場未來發展趨勢分析
未來TIL療法市場規模將進一步增長,行業監督監管更加完善,新一代TIL療法有望滿足更多臨床需求,產品可及性和接受度提高,目前國內已經涌現出一批創新能力與技術實力可與國際水平同臺競技的企業,其具有創新優勢和臨床優勢的產品將有望在全球競爭中占據一定的市場份額。
來源:沙利文分析
汪鵬
沙利文大中華區生命科學事業部項目經理
郵箱:aaron.wang@frostchina.com
楊澤鈺
沙利文大中華區生命科學事業部咨詢顧問
郵箱: Zeyu.Yang@frostchina.com
免責聲明:市場有風險,選擇需謹慎!此文僅供參考,不作買賣依據。
關鍵詞:
新聞發布平臺 |科極網 |環球周刊網 |中國創投網 |教體產業網 |中國商界網 |萬能百科 |薄荷網 |資訊_時尚網 |連州財經網 |劇情啦 |5元服裝包郵 |中華網河南 |網購省錢平臺 |海淘返利 |太平洋裝修網 |勵普網校 |九十三度白茶網 |商標注冊 |專利申請 |啟哈號 |速挖投訴平臺 |深度財經網 |深圳熱線 |財報網 |財報網 |財報網 |咕嚕財經 |太原熱線 |電路維修 |防水補漏 |水管維修 |墻面翻修 |舊房維修 |參考經濟網 |中原網視臺 |財經產業網 |全球經濟網 |消費導報網 |外貿網 |重播網 |國際財經網 |星島中文網 |手機測評 |品牌推廣 |名律網 |項目大全 |整形資訊 |整形新聞 |美麗網 |佳人網 |稅法網 |法務網 |法律服務 |法律咨詢 |成報網 |媒體采購網 |聚焦網 |參考網 |熱點網
中國資本網 版權所有
Copyright © 2011-2020 亞洲資本網 All Rights Reserved. 聯系網站:55 16 53 8 @qq.com